การประเมินคุณภาพชุดตรวจวิเคราะห์พิษของเชื้อคลอสตริเดียมดิฟฟิไซล์ เอ/บี โดยวิธีเลทเธอรัลโฟลอิมมูโนโครมาโตกราฟฟี
Main Article Content
บทคัดย่อ
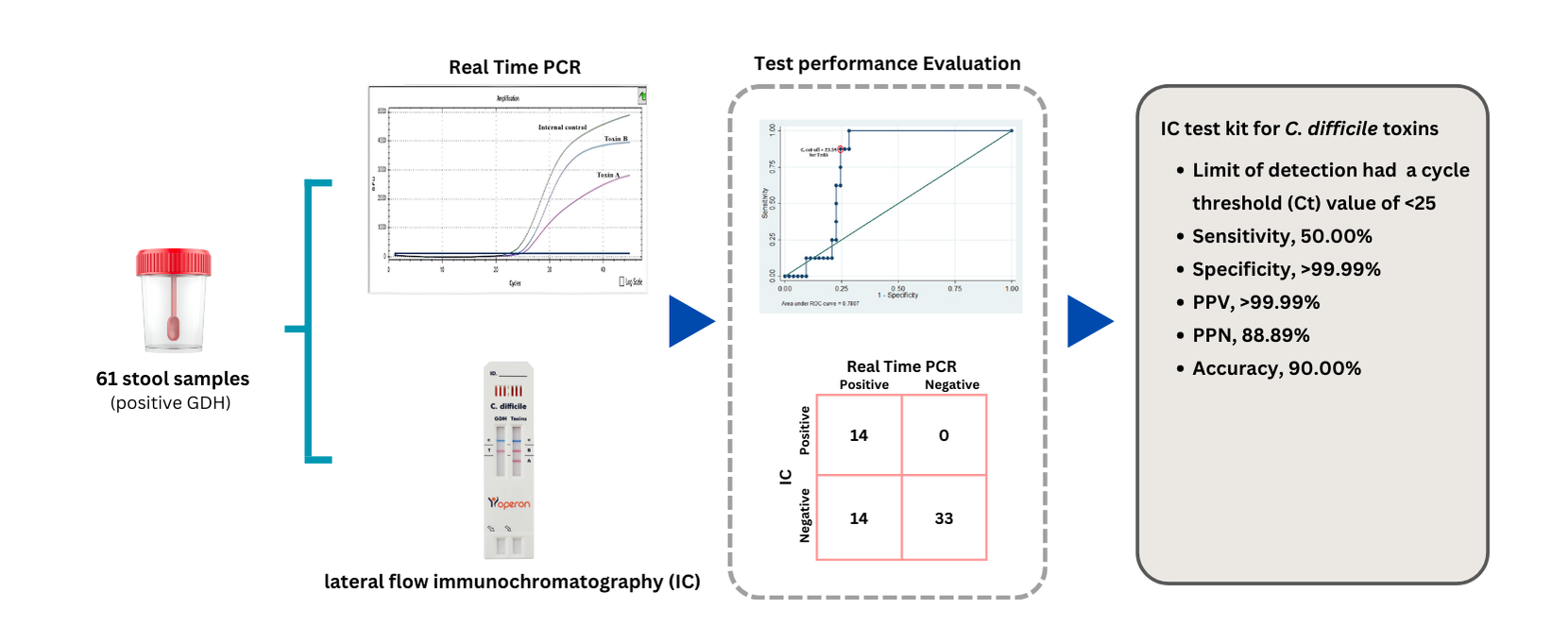
เชื้อ Clostridium หรือ Clostridiodes difficile ผลิตสารพิษทั้งชนิด A (TcdA) และ B (TcdB) เป็นสาเหตุของโรค CDI (C. difficile infection: CDI) ผู้ป่วยที่ติดเชื้อมีอาการท้องเสียอย่างรุนแรงจนถึงขั้นเสียชีวิต การตรวจ Glutamate dehydrogenase (GDH), TcdA และTcdB ของเชื้อด้วยวิธี Lateral flow Immunochromatography (IC) ในห้องปฏิบัติการจำเป็นต้องมีการประเมินคุณภาพของชุดตรวจวิเคราะห์สำหรับการนำมาใช้ การศึกษานี้มีวัตถุประสงค์เพื่อประเมินคุณภาพของชุดตรวจวิธี IC ที่ใช้อยู่ โดยใช้อุจจาระหลังจากตรวจประจำวันจากผู้ป่วยของโรงพยาบาลธรรมศาสตร์เฉลิมพระเกียรติ จ.ปทุมธานี จำนวน 61 ตัวอย่าง ทำการทดสอบ GDH, TcdA และ TcdB ด้วยวิธี IC และทดสอบยืนยันการพบเชื้อ C. difficile และเชื้อผลิตพิษชนิด TcdA และ TcdB ด้วยวิธี Real-time Polymerase Chain Reaction (Real-time PCR) ผลการทดลองยืนยันการพบเชื้อ C. difficile ในอุจจาระทั้งหมด (ร้อยละ 100.00) และเชื้อผลิตพิษชนิด TcdA+/TcdB+, TcdA-/TcdB+ เท่ากับร้อยละ 37.70 และ 8.20 และเชื้อชนิดไม่ผลิตพิษ (TcdA-/TcdB-) เท่ากับร้อยละ 54.10 ตามลำดับ สำหรับคุณภาพของชุดทดสอบวิธี IC ที่ใช้สำหรับกลุ่มผู้ป่วย CDI มีความไว ความจำเพาะ PPV NPV ความถูกต้อง สำหรับการตรวจพิษชนิด TcdA/TcdB เท่ากับร้อยละ 50.00, >99.99, >99.99, 88.89, 90.00 ตามลำดับและค่า Cycle threshold (Ct) สำหรับ TcdA และ TcdB อยู่ที่ 23.59 และ 24.43 ตามลำดับ สรุปว่าชุดตรวจวิเคราะห์ GDH, TcdA/B ของวิธี IC มีคุณภาพสามารถยอมรับได้และควรใช้วิธี Real-time PCR เพื่อตรวจวิเคราะห์ยืนยัน
Article Details
เอกสารอ้างอิง
Bacci, S., Mølbak, K., Kjeldsen, M. K. and Olsen,K.E.,2011,Binary toxinand death after Clostridium difficile infection, Emerg. Infect. Dis. 17(6): 976–982.
Berry, C. E., Davies, K. A., Owens, D. W. and Wilcox, M. H., 2017, Is there a relationship between the presenceof the binary toxingenes in Clostridium difficile strains and the severity of C. difficile infection (CDI)?, Eur. J. Clin. Microbiol. Infect. Dis. 36(12): 2405–2415.
Imwattana, K., Wangroongsarb, P. and Riley, T. V., 2019, High prevalence and diversity of tcdA-negative and tcdB-positive, and non-toxigenic, Clostridium difficile in Thailand, Anaerobe. 57: 4–10.
Imwattana, K., Knight, D. R., Kullin, B., Collins, D. A. and Putsathit, P., 2019, Clostridium difficile ribotype 017 - characterization, evolution and epidemiology of the dominant strain in Asia, Emerg. Microbes. infect. 8(1): 796–807.
Sholeh, M., Kouhsari, E., Talebi, M., Hallajzadeh, M. and Godarzi, F., 2021, Toxin gene profiles and antimicrobial resistance of Clostridioides difficile infection: a single tertiary care center study in Iran, Iran. J. Microbiol. 13(6): 793–800.
Cohen, S. H., Tang, Y. J., Hansen, B. and Silva, J., Jr., 1998, Isolation of a toxin B-deficient mutant strain of Clostridium difficile in a case of recurrent C. difficileassociated diarrhea, Clin. Infect. Dis.26(2): 410–412.
Drudy, D., Harnedy, N., Fanning, S., O'Mahony,R.and Kyne,L.,2007, Isolation and characterizationof toxin A-negative, toxin B-positive Clostridium difficile in Dublin, Ireland, Clin. Microbiol. Infect. 13(3): 298–304.
Humphries,R. M., Uslan, D. Z. and Rubin, Z., 2013, Performance of Clostridium difficile toxinenzyme immunoassay and nucleic acid amplificationtests stratified by patient disease severity, J. Clin. Microbiol. 51(3): 869–873.
Operon Immuno and Molecular Diagnostics, 2025, Simple GDH-Toxins, Available Source :https://www.operondx.com/wp-content/uploads/pdf/instructions/0905144_GDH-Toxins_web.pdf, February 21, 2025.
Certest Biotec SL, Viasure Clostridium Difficile Real-Time PCR Detection Kit, Available Source :https://www.certest.es/wp-content/uploads/2015/12/VIASUREClostridium-difficile-EN.pdf, February 21,2024.
Certest Biotec SL, Viasure Clostridium Difficile Toxin A+B Real-Time PCR Detection Kit, Available Source: https://www.certest.es/wp-content/uploads/2015/12/VIASURE_ClostridiumdifficiletoxAB_EN.pdf,February21,2024.
Medcalc Software Ltd, Diagnostic Test Evaluation Calculator, Available Source: https://www.medcalc.org/calc/diagnostic_test.php (version22.021), May 9, 2024.
Nahm, F. S., 2022, Receiver operating characteristic curve: overview and practical use for clinicians, Korean J. Anesthesiol. 75(1): 25–36.
Polage, C. R., Gyorke, C. E., Kennedy, M. A., Leslie, J. L. and Chin, D. L., 2015, Overdiagnosis of Clostridium difficile infectioninthe molecular testera, JAMA. Intern. Med. 175(11): 1792–1801.
Putsathit,P., Kiratisin,P., Ngamwongsatit, P. and Riley, T. V., 2015, Clostridium difficile infection in Thailand, Intern. J. Antimicrob. Agents. 45(1): 1–7.
Wongwanich,S., Pongpech,P., Dhiraputra, C., Huttayananont,S. and Sawanpanyalert, P., 2001, Characteristics of Clostridium difficile strains isolated from asymptomatic individuals and from diarrheal patients, Clin. Microbiol. Infect.7(8): 438–441.
Putsathit, P., Maneerattanaporn, M., Piewngam,P., Kiratisin,P. and Riley,T.V., 2016, Prevalence and molecular epidemiology of Clostridium difficile infection in Thailand, New. Microbes. New. Infect. 15: 27–32.
Wongkuna, S., Janvilisri, T., Phanchana, M., Harnvoravongchai, P. and Aroonnual, A., 2021, Temporal variations in patterns of Clostridioides difficile strain diversity and antibiotic resistance in Thailand, Antibiotics. 10(6): 1-15.
Wongwanich, S., Ramsiri, S., Vanasin, B., Khowsaphit, P. and Tantipatayangkul, P., 1990, Clostridium difficile associated disease in Thailand, Southeast. Asian. J. Trop. Med. Pub. Health. 21(3): 367–372.
Issarachaikull, R., Khantipong, M., Sawatpanich, A. and Suankratay, C., 2015, Prospective evaluation of a novel two-step protocol for screeningof Clostridium difficile infection in hospitalized adult patients, Southeast. Asian. J. Trop. Med. Pub. Health. 46(6): 1037–1048.
Chapin,K. C., Dickenson,R. A., Wu,F.and Andrea, S. B., 2011, Comparison of five assays for detection of Clostridium difficile toxin, J. Mol. Diagn. 13(4): 395–400.
Jaqueti, A. J., Molina, E. L. M., García-Arata, I., García-Martínez, J. and Cano De Torres, I., 2021, Significance of a polymerase chain reaction method inthe detection of Clostridioides difficile, Rev. Esp. Quimioter. 34(2): 141–144.
Fedorko, D.P., Engler, H. D., O'Shaughnessy, E. M., Williams, E. C. and Reichelderfer, C. J., 1999, Evaluationof tworapid assays for detectionof Clostridium difficiletoxin A in stool specimens, J. Clin. Microbiol. 37(9): 3044–3047.
René, P., Frenette, C. P., Schiller, I., Dendukuri, N. and Brassard, P., 2012, Comparison of eight commercial enzyme immunoassays for the detection of Clostridium difficile from stool samples and effect of strain type, Diagn. Microb. Infect. Dis. 73: 94–96.
Eastwood, K., Else, P., Charlett, A. and Wilcox, M., 2009, Comparison of nine commercially available Clostridium difficile toxin detection assays, a real-time PCR assay for C. difficile tcdB, and a glutamate dehydrogenase detection assay to cytotoxin testing and cytotoxigenic culture methods, J. Clin. Microb. 47(10): 3211–3217.
Burnham, C. A. and Carroll, K. C., 2013, Diagnosisof Clostridium difficileinfection: anongoing conundrum for clinicians and for clinical laboratories, Clin. Microbiol. Rev. 26(3): 604–630.
Alcalá, H. L., Reigadas, R. E. and Bouza, S. E., 2017, Clostridium difficileinfection, Med. Clin. 148(10): 456–463.
Lee, S., Nanda, N., Yamaguchi, K., Lee, Y. and She, R. C., 2022, Clostridioides difficile Toxin B pcr cycle threshold as a predictor of toxin testing in stool specimens from hospitalized adults, Antibiotics. 11(5): 1-9.