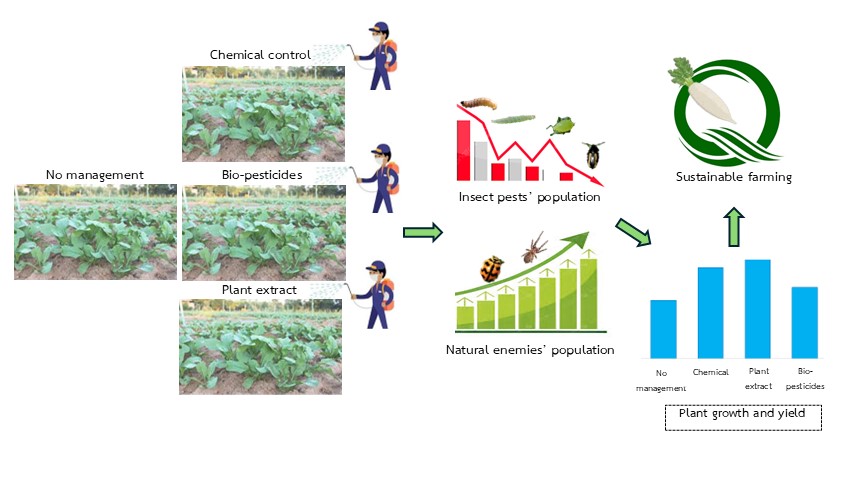
ผลของวิธีการจัดการศัตรูพืชต่อปริมาณแมลงศัตรู การเจริญเติบโตและผลผลิตผักกาดหัว
Main Article Content
บทคัดย่อ
ในกระบวนการผลิตพืชมักประสบปัญหาการเข้าทำลายจากแมลงศัตรูพืช การเลือกวิธีการป้องกันกำจัดที่มีประสิทธิภาพจึงเป็นปัจจัยสำคัญที่มีผลโดยตรงต่อปริมาณผลผลิต งานวิจัยนี้มีวัตถุประสงค์เพื่อศึกษาผลของวิธีการจัดการศัตรูผักกาดหัว คือ ไม่มีการจัดการศัตรูพืช การจัดการแบบใช้สารเคมี การจัดการโดยใช้สารสกัดจากพืชและการจัดการโดยสารชีวภัณฑ์กำจัดศัตรูพืช ผลการศึกษาพบว่า กรรมวิธีการจัดการศัตรูพืชมีแนวโน้มทำให้แมลงศัตรูพืชชนิดทำลายใบมีปริมาณลดลงลง แต่ไม่มีผลกับแมลงที่อาศัยทำลายอยู่ภายในต้นพืช กรรมวิธีการจัดการด้วยสารสกัดจากพืชมีผลต่อการเจริญเติบโตของผักกาดหัวอย่างมีนัยสำคัญทางสถิติ โดยมีความกว้างและความยาวใบสูงที่สุด เท่ากับ 5.94±0.54 และ 16.52±0.99 เซนติเมตร ตามลำดับ แตกต่างอย่างมีนัยสำคัญยิ่งกับกรรมวิธีการใช้สารเคมีและแปลงที่ไม่มีการจัดการศัตรูพืช แต่ไม่แตกต่างกับกรรมวิธีการใช้สารชีวภัณฑ์ นอกจากนี้แปลงที่มีการใช้สารสกัดจากพืช ให้น้ำหนักผักกาดหัวและผลผลิตต่อไร่สูงที่สุด เท่ากับ 244.67±27.39 กรัม/หัว และ 2,348.8±262.91 กิโลกรัม/ไร่ ตามลำดับ แตกต่างกันอย่างมีนัยสำคัญยิ่งทางสถิติกับกรรมการใช้สารชีวภัณฑ์ การใช้สารเคมีและไม่มีการจัดการศัตรูพืช โดยกรรมวิธีที่ไม่มีการจัดการศัตรูพืชมีน้ำหนักหัวและผลผลิตน้อยที่สุด วิธีนี้เป็นอีกทางเลือกที่ยั่งยืนในการควบคุมศัตรูพืช
Article Details
เอกสารอ้างอิง
Jakmatakul, R., Suttisri, R. and Tengamnuay, P., 2009, Evaluation of antityrosinase and antioxidant activities of Raphanus sativus root: Comparison between freeze-dried juice and methanolic extract, Thai J. Pharm. Sci. 33: 22-30.
Department of Agricultural Extension 2016, The Situation of Radish Cultivation by Province, Available Source: http://productive.doae.go.th, August 30, 2024. (in Thai)
Daungtisan, J., Pongprasert, W., Buranapanichpan, S. and Tayutivutikul, J., 2007, Biology and ecology of striped flea beetle in lower northern Thailand, Kamphaengsean Acad. J. 5: 20-29. (in Thai)
Athipanyakul, T., 2012, Expected utility theory and prospect theory: Attitude and decision-making behavior toward risk of farmers, Khonkaen Agr. J. 40: 269-278. (in Thai)
Isman, M.B., 2019, Challenges of pest management in the twenty first century: New tools and strategies to combat old and new foes alike, Front. Agron. 1: 1-4.
Burana, K. and Nimkingrat, P., 2023, Effect of bio-products in controlling common cutworm Spodoptera litura Fabricius (Lepidoptera: Noctuidae) in marigolds, Khonkaen Agr. J. 51(2): 332-345. (in Thai)
Mahamud, M.R., 2019, Large Scale production and increased shelf life of Trichoderma Harzianum inoculums in semi solid medium, Malays. J. Sustain. Agric. 3(1): 5-7.
Wongsuk, S., Chanbang, Y. and Kulsarin, J., 2017, Efficacy of fine tobacco leaf scrap and stem for controlling some insect pests of vegetables, J. Agric. 33(3): 367-376.
Rassami, W., Bunroj, A., Ormking, C. and Iamjitkusol, S., 2019, Study on integrated insect pest management in pesticide residue free crop in Khao Khitchakut district, Chathaburi province, Rambhai Barni Res. J. 14: 82-87. (in Thai)
Divekar, P.A., Majumder S., Halder, J., Kedar, S.C. and Singh, V., 2024, Sustainable pest management in cabbage using botanicals: Characterization, effectiveness and economic appraisal, J. Plant Dis. Prot. 131: 113-130.
Sivapragasam, A., 2017, Ecological and foraging aspects of the cabbage webworm, Hellula undalis Fabricius, Malays. J. Sustain. Agric. 51: 53-58.
Mkindi, A.G., Tembo, Y.L.B., Mbega, E.R., Smith, A.K., Farrell, I.W., Ndakidemi, P.A., Stevenson P.C. and Belmain, S.R., 2020, Extracts of common pesticidal plants increase plant growth and yield in common bean plants, Plants. 9(2): 149.
Mutale-joan, C., Redouane, B., Najib, E., Yassine, K., Lyamlouli, K., Laila, S., Zeroual, Y. and Hicham, E.A., 2020, Screening of microalgae liquid extracts for their bio stimulant properties on plant growth, nutrient uptake and metabolite profile of Solanum lycopersicum L., Sci Rep. 10: 2820.
Sumardi, D., Bahariawan, M., Maulani, R.R., Suhandono, S., Novia, C., Harahap, A.F.P. and Gozan, M., 2021, The effect of concentration of tobacco (Nicotiana tabacum) extract on growth parameters of rice (Oryza sativa) inpari-32, IOP Conf. Ser.: Earth Environ. Sci. 940: 1-9.
Petkova, M., Petrova, S., Spasova Apostolova, V. and Naydenov, M., 2022, Tobacco plant growth-promoting and antifungal activities of three endophytic yeast strains, Plants. 11(6): 751.
Capdesuñer, Y., Linares, C., Schöne, J., El-Hasan, A., Vögele, R., Yanes-Paz, E., Ortega-Delgado, E., Martínez-Montero, M. E., Rodríguez, E. and Quiñones-Gálvez, J., 2023, Tobacco leaf-surface extracts: Antimicrobial potential against phytopathogenic fungi and in vitro culture bacterial contaminants, Int. J. Plant Biol. 14(4): 1017-1033.
Shi, M., Hao, S., Wang, Y., Zhang, S., Zhou, W., Chen, H., 2024, Plant growth promoting fungi improve tobacco yield and chemical components by reassembling rhizosphere fungal microbiome and recruiting probiotic taxa, Environ. Microbiome. 19: 83.
Zhong, J., Pan, W., Jiang, S., Hu, Y., Yang, G., Zhang, K., Xia, Z. and Chen, B., 2024, Flue-cured tobacco intercropping with insectary floral plants improves rhizosphere soil microbial communities and chemical properties of flue-cured tobacco, BMC Microbiol. 24: 446.
Farooq, M., Hussain, T., Wakeel, A. and Cheema, Z.A., 2014, Differential response of maize and mungbean to tobacco allelopathy, Exp. Agric. 50(4): 611-624.
Kanmani, S., Kumar, L., Raveen, R., Tennyson, S., Arivoli, S. and Jayakumar, M., 2021, Toxicity of tobacco Nicotiana tabacum Linnaeus (Solanaceae) leaf extracts to the rice weevil Sitophilus oryzae Linnaeus 1763 (Coleoptera: Curculionidae), J. Basic Appl. Zool. 82(1): 1-10.
Sarker, S. and Lim, U.T., 2018, Extract of Nicotiana tabacum as a potential control agent of Grapholita molesta (Lepidoptera:Tortricidae), Plos one. 13(8): e0198302.
Khan, B.S., Shahzad, M.A., Ashraf, M.I., Sarwar, Z.M., Farooq, M. and Rasool, A., 2024, Evaluation of five different botanical extracts against some pests and predators in laboratory conditions, Pak. J. Agri. Res. 37(1): 62-69.
Xie, M., Zhong, Y., Lin, L., Zhang, G., Wei, N., Zhang, F. and Chen, H., 2025, Comprehensive transcriptome and metabolome analysis of the adaptability and detoxification ability of Spodoptera frugiperda larvae to tobacco, J. Insect Physiol. 163: 104800.
Pradinata, R., Ginting, T.Y. and Amrul, H.M.Z., 2024, Effectiveness of biopesticides Nicotiana tabacum L and Ageratum conyzoides L as controlling Spodoptera exigua in red onion (Allium ascalonicum L.), J. Pembela. Biol. Nucl. 10(1): 219-229.