การคัดกรองโรคมะเร็งปอดในกลุ่มประชากรอายุ 55-75 ปี ด้วยวิธีการตรวจวิธีภาพรังสีคอมพิวเตอร์ แบบใช้ปริมาณรังสีต่ำ กรณีศึกษานำร่อง โรงพยาบาลเชียงคำ จังหวัดพะเยา
คำสำคัญ:
การคัดกรองมะเร็งปอด, ภาพถ่ายเอกซเรย์ทรวงอกดิจิดัล (CXR AI), เอกซเรย์คอมพิวเตอร์ปริมาณรังสีขนาดตํ่า (LDCT)บทคัดย่อ
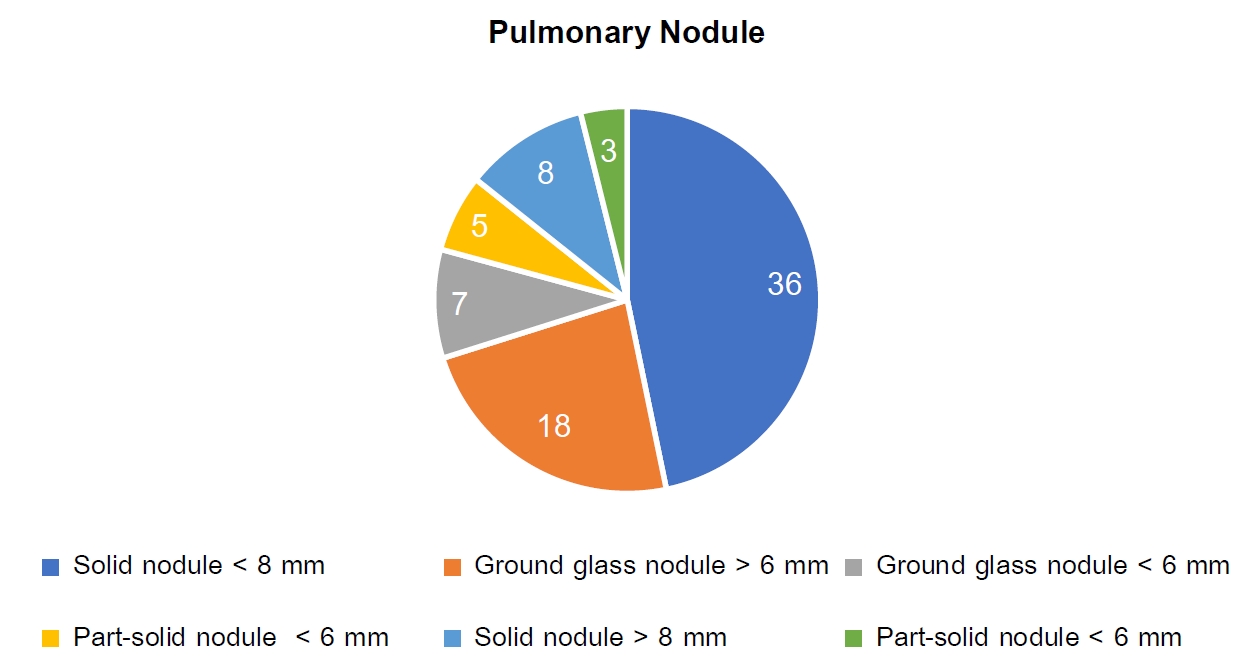
การวิจัยครั้งนี้ เพื่อสำรวจความชุกของมะเร็งปอดด้วยการคัดกรองด้วยวิธีภาพรังสีคอมพิวเตอร์ แบบใช้ปริมาณรังสีตํ่า (Low-dose computerized tomography) LDCT ในประชากรกลุ่มเสี่ยง และเพื่อศึกษาปัจจัยที่สัมพันธ์ต่อการเกิดโรคมะเร็งปอดและประเมินความเสี่ยงโอกาสของการเกิดโรคมะเร็งปอด ทำการศึกษาแบบภาคตัดขวาง (Cross-Sectional Observational Pilot Study) ในประชากรคนไทย ที่มีอายุ 55-75 ปี ในอำเภอเชียงคำ จังหวัดพะเยา ในช่วงระหว่างวันที่ 3 สิงหาคม 2567 - 31 ธันวาคม 2567 จำนวน 100 คน เครื่องมือที่ใช้ประกอบด้วย แบบบันทึกข้อมูลของผู้ป่วยและปัจจัยเสี่ยงที่สำคัญ และแบบบันทึกผลการตรวจภาพถ่ายเอกซเรย์ทรวงอกดิจิทัล (CXR AI) และภาพเอกซเรย์คอมพิวเตอร์ ปริมาณรังสีขนาดตํ่า (LDCT) วิเคราะห์ความสัมพันธ์ความผิดปกติจาก LDCT ความเสี่ยงสูง โดยกําหนดนัยสําคัญทางสถิติ โดยใช้ค่า p < 0.050 โดยพบว่าอายุเฉลี่ยของผู้เข้าร่วมงานวิจัย 64 ปี ตรวจพบผลการอ่าน CXR AI ผิดปกติร้อยละ 72 พบมีลักษณะ Lung nodule คิดเป็นร้อยละ 18 และความผิดปกติ High risk LDCT: Lung-RADS ตั้งแต่ Category 3 ขึ้นไป ร้อยละ 14 ส่วนผลการตรวจพบความผิดปกติของผล LDCT (category) ที่พบบ่อยได้แก่ solid nodule ร้อยละ 75 ประกอบด้วย solid nodule <8 mm คิดเป็นส่วนใหญ่เป็นร้อยละ 36 ปัจจัยที่สัมพันธ์ต่อการเกิดโรคมะเร็งปอดและประเมินความเสี่ยงโอกาสของการเกิดโรคมะเร็งปอด ในประชากรกลุ่มเสี่ยง คือ การมีประวัติการใช้ประวัติสารระเหย สารอินทรีย์ (odds ratio [OR] 9.59, 95% confidence interval [CI] (1.33-70.16) p= 0.02) รวมถึงมีแนวโน้มเพิ่มขึ้นในกลุ่มที่ดื่มสุรา [OR] 7.735, [CI] (0.859-69.631) p=0.068 และมีอายุมากขึ้น [OR] 1.16, [CI] (0.997-1.350) p=0.054 และการนำ CXR AI มาใช้ในการคัดกรองเบื้องต้นจะเพิ่มโอกาสการตรวจพบความผิดปกติของการตรวจ LDCT โดยมี Sensitivity 100 % Specificity 32.56 % NPV 100% PPV 19.44% ตามลำดับ
เอกสารอ้างอิง
Siriwiwattnakul N. HOSPITAL-BASED CANCER REGISTRY 2022. Bangkok: National Cancer Institute; 2024. p.1-83.
Jayes L, Haslam PL, Gratziou CG, Powell P, Britton J, Vardavas C, et al. SmokeHaz: Systematic Reviews and Meta-analyses of the Effects of Smoking on Respiratory Health. Chest 2016;150(1):164-79.
Hill W, Lim LE, Weeden EC, Lee C, Augustine M, Chen K, et al. Lung adenocarcinoma promotion by air pollutants. Nature 2023;616(7955):159-67.
Rojanamatin J, Sangrajrang S, editors. Cancer in Thailand 2016-2018.10th ed. Bangkok: National Cancer Institute; 2021. p.1-170.
Bonney A, Malouf R, Marchal C, Manners D, Fong KM, Marshall HM, et al. Impact of low-dose computed tomography (LDCT) screening on lung cancer-related mortality. Cochrane Database Syst Rev 2022;8(8).
Tammemägi MC, Darling GE, Schmidt H, Walker MJ, Langer D, Leung YW, et al. Risk-based lung cancer screening performance in a universal healthcare setting. Nat Med 2024;30(4):1054-64.
Tammemägi MC. Selecting lung cancer screenees using risk prediction models-where do we go from here. Transl Lung Cancer Res 2018;7(3):243-53.
Tammemägi MC, Katki HA, Hocking WG, Church TR, Caporaso N, Kvale PA, et al. Selection criteria for lung-cancer screening. N Engl J Med 2013;368(8):728-36.
Marcus MW, Chen Y, Raji OY, Duffy SW, Field JK, et al. LLPi: Liverpool Lung Project Risk Prediction Model for Lung Cancer Incidence. Cancer Prev Res (Phila) 2015;8(6):570-5.
Sasieni D. editors. The Standard Protocol was developed by the NHS Cancer Programme with the CT Screening. 2nd ed. NHS England; 2022. p.1-40.
Lee JW, Kim HY, Goo JM, Kim EY, Lee SJ, Kim TJ, et al. Radiological Report of Pilot Study for the Korean Lung Cancer Screening (K-LUCAS) Project: Feasibility of Implementing Lung Imaging Reporting and Data System. Korean J Radiol 2018;19(4):803-8.
Triphuridet N, Singharuksa S, Vidhyakorn S. Practical difficulty of low dose computerized tomography as a lung cancer screening tool in an endemic area of tuberculosis. J Thorac Oncol 2017; 12(1): S568-S9.
Thai AA, Solomon BJ, Sequist LV, Gainor JF, Heist RS, et al. Lung cancer. Lancet 2021;398(10299):535-54.
Hussain MdS, Gupta G, Mishra R, Patel N, Gupta S, Alzarea SI, et al. Unlocking the secrets: Volatile Organic Compounds (VOCs) and their devastating effects on lung cancer. Pathol Res Pract 2024; 255:155-7.
Hamashima C. Cancer screening guidelines and policy making: 15 years of experience in cancer screening guideline development in Japan. Jpn J Clin Oncol. 2018;48(3):278-86.
Chutivanidchayakul F, Suwatanapongched T, Petnak T. Clinical and chest radiographic features of missed lung cancer and their association with patient outcomes. Clin Imaging 2023; 99:73-81.
Upaisilsathaporn P, Klawandee S, Wanchaijiraboon P. The Potential of Chest X-Ray Artificial Intelligence Detecting Missed Lung Cancer Diagnosis in a Community Based Cancer in Thailand.
J Thorac Oncol 2024; 19(10): S473-S74.
ดาวน์โหลด
เผยแพร่แล้ว
รูปแบบการอ้างอิง
ฉบับ
ประเภทบทความ
สัญญาอนุญาต
ลิขสิทธิ์ (c) 2025 มหาวิทยาลัยพะเยา

อนุญาตภายใต้เงื่อนไข Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License.
ผู้นิพนธ์ต้องรับผิดชอบข้อความในบทนิพนธ์ของตน มหาวิทยาลัยพะเยา ไม่จำเป็นต้องเห็นด้วยกับบทความที่ตีพิมพ์เสมอไป ผู้สนใจสามารถคัดลอก และนำไปใช้ได้ แต่จะต้องขออนุมัติเจ้าของ และได้รับการอนุมัติเป็นลายลักษณ์อักษรก่อน พร้อมกับมีการอ้างอิงและกล่าวคำขอบคุณให้ถูกต้องด้วย







