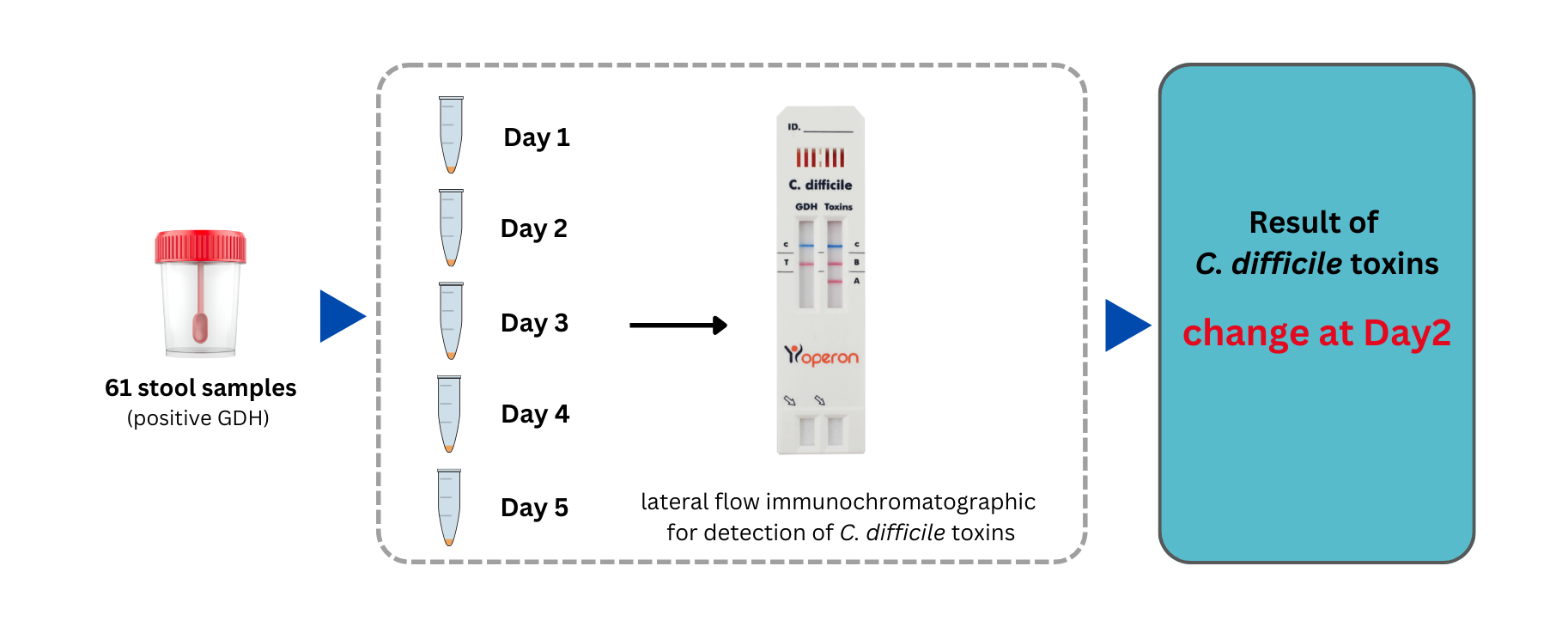
การศึกษาการเปลี่ยนแปลงของผลการตรวจวิเคราะห์พิษของเชื้อคลอสตริเดียมดิฟฟิไซล์ เอ/บี โดยวิธีเลทเธอรัลโฟลอิมมูโนโครมาโตกราฟฟี
Main Article Content
บทคัดย่อ
พิษของเชื้อ Clostridium หรือ Clostridiodes difficile (C. difficile) ชนิด A(TcdA) และ B(TcdB) ทำให้ผู้ป่วยเกิดอาการท้องเสียรุนแรงขั้นเสียชีวิตได้ การตรวจ Glutamate dehydrogenase (GDH) TcdAและ TcdB ของเชื้อด้วยวิธี Lateral flow immunochromatography (IC) หากไม่สามารถตรวจได้ทันทีต้องเก็บอุจจาระที่ 4°C เพื่อรอตรวจบางครั้งอาจนานถึง 5 วัน (Day1-5) การศึกษานี้มีวัตถุประสงค์เพื่อศึกษาหาวันที่เริ่มมีการเปลี่ยนแปลง (Critical day) ของผลตรวจ GDH, TcdA และ TcdB จากวันแรก (Day1) โดยใช้อุจจาระหลังจากตรวจประจำวันจากผู้ป่วยของโรงพยาบาลธรรมศาสตร์เฉลิมพระเกียรติ จ.ปทุมธานี จำนวน 61 ตัวอย่าง โดยแบ่งอุจจาระเก็บไว้ที่อุณหภูมิ 4°C เพื่อทำการตรวจ GDH, TcdA และ TcdB ด้วยวิธี IC ในวันที่ 2 ถึง 5 (Day2-5) จากนั้นวิเคราะห์ความสอดคล้องของผลจากวิธี IC ระหว่างวัน (Day1-5) ด้วย Cohen’s Kappa coefficient ผลการทดลองพบว่า Critical day เท่ากับ 2 เนื่องจากเป็นวันที่เริ่มมีการเปลี่ยนแปลงของผล GDH, TcdA และ TcdB สำหรับรูปแบบการรายงานผลตรวจ (ประกอบด้วย GDH/TcdA/TcdB เรียงกัน) ของวิธี IC(Day1 vs Day2-5) ยังมีความสอดคล้องกันในระดับ Almost perfect แต่ใน Day2-5 อาจปรากฎรูปแบบของผลตรวจที่ทำให้ผู้ป่วยพลาดการรักษาตั้งแต่ร้อยละ 4.90 ถึงร้อยละ 6.60 ได้ สรุปว่าการตรวจ GDH, TcdA/B ด้วยวิธี IC ควรตรวจทันทีภายใน 1 วันสามารถช่วยลดอัตราการเสียชีวิตของผู้ป่วยได้
Article Details
เอกสารอ้างอิง
Janoir, C., 2016, Virulence factors of Clostridium difficile and their role during infection, Anaerobe. 37: 13–24.
Putsathit, P., Maneerattanaporn, M., Piewngam, P., Knight, D. R. and Riley, T. V., 2017, Antimicrobial susceptibility of Clostridium difficile isolated in Thailand, Antimicrob. Resist. Infect. Control. 6: 1-6.
Imwattana, K., Putsathit, P., Leepattarakit, T., Kiratisin, P. and Riley, T. V., 2020, Mild or malign: clinical characteristics and outcomes of Clostridium difficile infection in Thailand, J. Clin. Microbiol. 58(9): 1217- 1220.
Imwattana, K., Wangroongsarb, P. and Riley, T. V., 2019, High prevalence and diversity of tcdA-negative and tcdB-positive and non-toxigenic Clostridium difficile in Thailand, Anaerobe. 57: 4–10.
Imwattana, K., Knight, D. R., Kullin, B., Collins, D. A., and Riley, T. V., 2019, Clostridium difficile ribotype 017 - characterization evolution and epidemiology of the dominant strain in Asia, Emerg. Microbes. Infect. 8: 796–807.
Sholeh, M., Kouhsari, E., Talebi, M., Hallajzadeh, M. and Amirmozafari, N., 2021, Toxin gene profiles and antimicrobial resistance of Clostridioides difficile infection: a single tertiary care center study in Iran, Iran. J. Microbiol. 13(6): 793–800.
Becker, S. L., Chatigre, J. K., Coulibaly, J. T., Mertens, P. and von Müller, L., 2015, Molecular and culture-based diagnosis of Clostridium difficile isolates from Côte d'Ivoire after prolonged storage at disrupted cold chain conditions, Trans. R. Soc. Trop. Med. Hyg. 109(10): 660–668.
Schora, D. M., Peterson, L. R. and Usacheva, E. A., 2018, Immunological stability of Clostridium difficile toxins in clinical specimens, Infect. Control. Hosp. Epidemiol. 39(4): 434–438.
Nho, S. W., Kim, M., Kim, S. J., Foley, S. L. and Cerniglia, C. E., 2021, Pragmatic strategy for fecal specimen storage and the corresponding test methods for Clostridioides difficile diagnosis, Pathogens. 10(8): 1-13.
Borriello, S. P., Vale, T., Brazier, J. S., Hyde, S. and Chippeck, E., 1992, Evaluation of a commercial enzyme immunoassay kit for the detection of Clostridium difficile toxin A, Eur. J. Clin. Microbiol. Infect. Dis. 11(4): 360–363.
Bowman, R. A. and Riley, T. V., 1986, Isolation of Clostridium difficile from stored specimens and comparative susceptibility of various tissue culture cell lines to cytotoxin, FEMS. Microbiol. Lett. 34: 31-35.
Planche, T., Aghaizu, A., Holliman, R., Riley, P. and Krishna, S., 2008, Diagnosis of Clostridium difficile infection by toxin detection kits: A systematic review, Lancet. Infect. Dis. 8(12): 777–784.
Operon immune and molecular diagnostics, 2025, Simple GDH-Toxins, Available Source: https://www.operondx.com/wpcontent/uploads/pdf/instructions/0905144_GDH-Toxins_web.pdf, February 21, 2025.
McHugh, M. L., 2012, Interrater reliability: The kappa statistic, Biochem. Med. 22(3): 276–282.
Kvach, E. J., Ferguson, D., Riska, P. F. and Landry, M. L., 2010, Comparison of BD GeneOhm C. diff real-time pcr assay with a two-step algorithm and a toxin A/B enzyme-linked immunosorbent assay for diagnosis of toxigenic Clostridium difficile infection, J. Clin. Microbiol. 48: 109–114.
Novak-Weekley, S. M., Marlowe, E. M., Miller, J. M., Cumpio, J. and Weissfeld, A., 2010, Clostridium difficile testing in the clinical laboratory by use of multiple testing algorithms, J. Clin. Microbiol. 48(3): 889–893.
Sharp, S. E., Ruden, L. O., Pohl, J. C., Hatcher, P. A. and Ivie, W. M., 2010, Evaluation of the C.Diff quik chek complete assay, a new glutamate dehydrogenase and A/B toxin combination lateral flow assay for use in rapid, simple diagnosis of Clostridium difficile disease, J. Clin. Microbiol. 48(6): 2082–2086.
Alcalá L., 2013, Laboratory tests for diagnosis of Clostridium difficile infection: past, present, and future, Enferm. Infecc. Microbiol. Clin. 31(2): 65–67.
Grześkowiak, Ł., Riedmüller, J., Vahjen, W. and Zentek, J., 2020, Storage procedures and time influence the detectability of Clostridium difficile toxin A but not toxin B in porcine fecal specimens, J. Vet. Diagn. Invest. 32(2): 222–225.
Aichinger, E., Schleck, C. D., Harmsen, W. S., Nyre, L. M. and Patel, R., 2008, Nonutility of repeat laboratory testing for detection of Clostridium difficile by use of pcr or enzyme immunoassay, J. clin. Microbiol. 46(11), 3795–3797.
Cardona, D. M. and Rand, K. H., 2008, Evaluation of repeat Clostridium difficile enzyme immunoassay testing, J. Clin. Microbiol. 46(11): 3686–3689.
Barbut, F., Surgers, L., Eckert, C., Visseaux, B. and Lalande, V., 2014, Does a rapid diagnosis of Clostridium difficile infection impact on quality of patient management?, Clin. Microbiol. Infect. 20(2): 136–144.
Freeman, J. and Wilcox, M. H., 2003, The effects of storage conditions on viability of Clostridium difficile vegetative cells and spores and toxin activity in human faeces, J. Clin. Pathol. 56(2): 126–128.
Barbut, F., Beaugerie, L., Delas, N., Fossati-Marchal, S. and Petit, J. C., 1999, Comparative value of colonic biopsy and intraluminal fluid culture for diagnosis of bacterial acute colitis in immunocompetent patients. infectious colitis study group, Clin. Microbiol. Infect. 29(2): 356–360.
Planche, T. D., Davies, K. A., Coen, P. G., Finney, J. M. and Wilcox, M. H., 2013, Differences in outcome according to Clostridium difficile testing method: a prospective multicentre diagnostic validation study of C difficile infection, Lancet. Infect. Dis. 13(11): 936–945.